|
|
| Un livre accompagne le site depuis octobre 2024. Découvrez-le ici > |  |
|
|
|
|
||||
|
|
||||||
|
|
|
|
|
|
Les bases moléculaires du toucher se précisent
| |
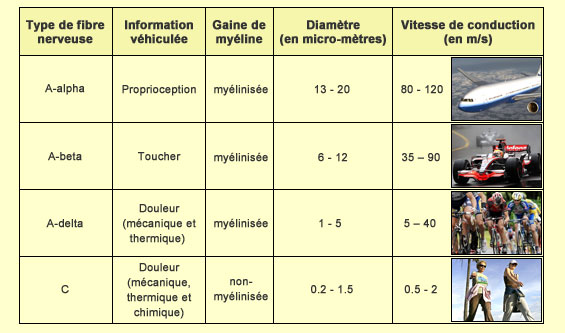
Vous vous fermez une porte sur un doigt. Vous vous cognez la jambe sur une chaise. Vous vous brûlez le bras sur une casserole encore chaude. À chaque fois, vous avez d'abord un réflexe de retrait, puis une sensation douloureuse aiguë suivie d'une douleur sourde. Avant de regarder les voies nerveuses qui amènent l'information douloureuse jusqu'au cerveau, regardons d'où part cette douleur et dans quel type de fibre nerveuse elle voyage. Cela est en effet essentiel pour comprendre ce que l'on appelle la douleur rapide (ou aiguë) et la douleur lente (ou sourde). D'abord, contrairement aux autres types de fibres sensorielles comme celle du toucher qui ont des structures spécialisées à leur extrémité (corpuscules de Pacini, de Messner, etc.), les fibres nociceptives n'ont aucune spécialisation de ce type. On dit qu'elles ont plutôt des " terminaisons libres " qui forment un maillage dense d'arborisations multiples considérées comme les nocicepteurs, c'est-à-dire les récepteurs sensoriels de la douleur. Ceux-ci ne répondent que lorsqu'un stimulus est d'une intensité suffisamment élevé pour menacer l'intégrité de l'organisme, autrement dit lorsqu'il est susceptible d'entraîner une lésion. Il existe différents types de ces fibres nerveuses dont les terminaisons libres forment les nocicepteurs. Toutes relient les organes périphériques à la moelle épinière, mais leur diamètre diffère grandement, de même que l'épaisseur de la gaine de myéline qui entoure la fibre nerveuse ou axone. Or le diamètre et la myélinisation influencent tous deux la vitesse de conduction de l'influx nerveux : plus le diamètre d'une fibre est grand, plus elle est alors myélinisée, et plus cette fibre conduira l'influx nerveux rapidement. Avec ces deux critères, on distingue les fibres sensorielles suivantes :
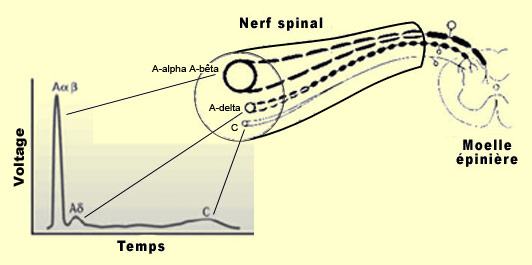
Les différentes vitesses de conduction des deux types de fibres nerveuses nociceptives (A-delta et C) expliquent la façon particulière dont on ressent la douleur lorsqu'on se blesse : d'abord une douleur aiguë, vive et précise qui fait place quelques secondes plus tard à une douleur plus diffuse et plus sourde. Ce délai provient directement de la vitesse de conduction différente des fibres A-delta et C qui fait que leur message n'atteint pas le cerveau exactement en même temps. Ce qu'on nomme la " douleur rapide ", qui disparaît assez vite, vient de la transmission d'influx nerveux dans les fibres A-delta (qui conduit l'influx nerveux à la vitesse d'un cycliste). Et la " douleur lente ", plus persistante, est issue de la stimulation des fibres C non myélinisée (qui conduit l'influx nerveux à la vitesse d'un marcheur). On estime que ces dernières comptent pour environ 70% des fibres nociceptives.
Ces deux composantes de la douleur vont emprunter des voies différentes, évolutivement parlant, pour se rendre jusqu'au cerveau : une voie plus récente (douleur rapide) et une voie plus ancienne (douleur lente). C'est aussi la composante rapide, par les fibres A-delta, qui permet à nos réflexes de retrait de se développer en quelques millisecondes, lorsque l'on marche sur un clou par exemple.
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Les voies ascendantes nociceptives sont formées de fibres A-delta et C peu ou pas myélinisées (comparé aux fibres tactiles et proprioceptives très myélinisées). Elles empruntent plusieurs voies d'origine évolutive plus ou moins anciennes afin de permettre la localisation et la connotation émotive désagréable de la douleur par le cerveau. On sait toutefois qu'il ne s'agit pas de voies rigides qui transmettent les messages nociceptifs intégralement et sans déformation de la périphérie jusqu'au cerveau. Les nocicepteurs peuvent être très activés sans qu'il y ait douleur, comme les soldats ou les sportifs blessés qui ne ressentent pratiquement pas la douleur dans le feu de l'action. Ou plus simplement, qui ne s'est pas déjà coupé sans s'en rendre compte parce que son attention était concentrée sur l'exécution d'une tâche prenante ? Sans parler de l'effet placebo, où le seul fait de croire en un traitement peut diminuer la douleur en l'absence de tout ingrédient actif… Pour comprendre ce qui rend possibles ces phénomènes, il faut s'intéresser à ce qu'on appelle " le contrôle descendant de la douleur ". Il s'agit de voies nerveuses qui vont descendre des structures centrales pour aller réduire le signal nociceptif en provenance du corps qui chemine dans les voies ascendantes. Bien que toutes nos perceptions soient sujettent, au moins à certains degrés, à des modulations d'origine centrale, c'est avec la perception de la douleur que ces mécanismes " de haut en bas " montrent toute leur puissance. Les mécanismes de contrôle descendants de la douleur pouvant aller, comme on l'a dit, jusqu'à faire disparaître complètement certaines formes de douleur. Le changement de paradigme est donc énorme. D'une part, il n'y a pas de ligne directe qui relierait des récepteurs de la douleur à des " centres de la douleur " dans le cerveau. Et d'autre part, les voies de la douleur sont mieux décrites en terme d'influences ascendantes et descendantes concomitantes : une véritable symphonie d'activité neuronale se produit simultanément dans les deux directions, et c'est la rupture de ce fragile équilibre en faveur des messages nociceptifs excitateurs qui produit la douleur. La douleur devient donc davantage une " opinion " que l'organisme se crée sur son intégrité physique qu'une réponse réflexe à une lésion. Cela a par exemple permis des avancées importantes dans le traitement de la douleur puisqu'on peut maintenant chercher à potentialiser ces voies descendantes qui inhibent la douleur. La théorie du portillon est celle qui est aujourd'hui reconnue pour décrire le mieux les mécanismes à l'œuvre dans le contrôle descendant de la douleur. Sa métaphore principale est celle de " portes " qui, tout au long des voies ascendantes de la douleur, peuvent se fermer pour rendre plus difficile le passage de l'influx nociceptif. Le même degré d'activité d'un nocicepteur ne va donc pas conduire à la perception de la même intensité douloureuse selon le degré d'ouverture de ces portes situées au niveau des principaux relais des voies de la douleur.
|
| |
|
|
|
|
|
|
|
|