|
|



|
|
| L'ATROPHIE CORTICALE DE L'ALZHEIMER |
|
Les signes cliniques
de l’Alzheimer s’expliquent en fonction des régions cérébrales
atrophiées successivement par la
dégénérescence neurofibrillaire et l’accumulation de
plaques amyloïdes. Ces deux marqueurs biologiques
associés à l’Alzheimer semblent se développer de manière
synergique. La neurotoxicité du peptide amyloïde concerne toutes les
régions cérébrales mais affecte, au
stade léger de l’Alzheimer, surtout les régions autour
de l’hippocampe où apparaît la dégénérescence
neurofibrillaire. Cette dégénérescence
causée par une pathologie des protéines
tau va alors s’intensifier sous l’influence (ou, pour reprendre
la représentation du schéma ci-bas, « sous le poids »)
des dysfonctionnements du peptide amyloïde. | 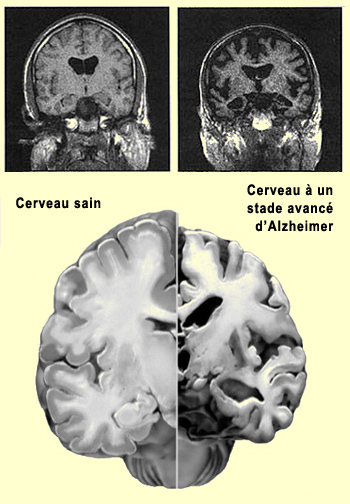 |
La dégénérescence neurofibrillaire
va ensuite s’étendre progressivement à d’autres régions
cérébrales selon une séquence donnée, hiérarchique
et invariable, qui s’explique par les connexions synaptiques que font ces
régions entre elles. La pathologie tau se développe ainsi en suivant
des voies anatomiques et non par diffusion passive. On
a défini 10 stades de la pathologie tau qui correspondent à 10 régions
cérébrales qui s’atrophient successivement (voir le schéma
ci-dessous). Les manifestations cliniques apparaissent généralement
vers le stade 5, 6 ou 7 quand les régions polymodales associatives, comme
le cortex pariétal, frontal antérieur et temporal supérieur,
commencent à être touchées. 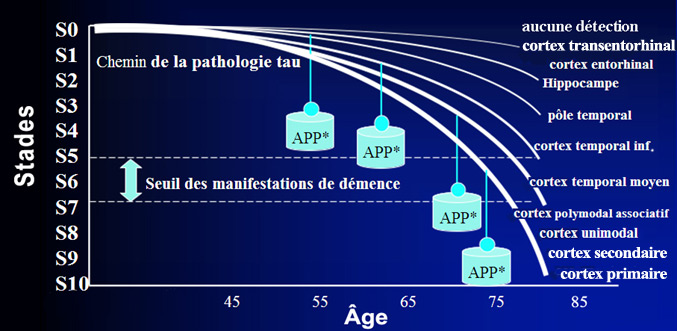
Les
icônes de poids marqués
APP* symbolisent le développement synergique de la pathologie des protéines
tau avec les plaques amyloïdes. Source
: www.lille.inserm.fr/u422 |
Le
seuil de manifestation clinique est certainement fluctuant et modulé par
de nombreux autres facteurs qui vont s’ajouter au dysfonctionnement des
protéines tau et amyloïde : diminution de facteurs trophiques,
présence de facteurs apoptotiques (voir capsule outil à gauche)
et de microinflammation, réaction astrocytaire et microgliale, stress oxydatif,
etc. Les effets néfastes de pathologies associées
peuvent aussi abaisser ou relever ce seuil, par exemple les pathologies vasculaires.
Et bien sûr, d’autres
facteurs environnementaux et génétiques qui influencent la vulnérabilité
neuronale (et par conséquent la « réserve neuronale »),
le bon développement des réseaux de neurones, etc.
Bien que l’imagerie cérébrale
ne permette pas de diagnostiquer l’Alzheimer ni d’en détecter
la présence avant les premiers symptômes, elle demeure un outil précieux
pour confirmer et comprendre l’évolution de l’atrophie cérébrale
qui lui est associée. Des résultats prometteurs
ont été obtenus avec les techniques d’imagerie classique comme
la tomographie par émission de positons (TEP) ou l’imagerie par résonance
magnétique (IRM) adaptées aux spécificités de l’Alzheimer. La
TEP permet par exemple de voir le taux d’absorption de glucose pour différentes
régions du cerveau, et donc de détecter s’il y a des régions
de moindre adsorption. Un aspect fort utile, puisque des recherches ont démontré
que les personnes aux premiers
stades de l’Alzheimer intègrent moins de glucose dans certaines
parties de leur cerveau. On utilise aussi la TEP avec
le marqueur PiB (pour « Pittsburgh compound B », en anglais),
une molécule fluorescente qui se lie au peptide
bêta-amyloïde et permet donc de visualiser la présence de
plaques amyloïdes associées à l’Alzheimer. Avec
l’IRM, on peut par exemple observer l'atrophie de l'hippocampe au fil du
temps, en se basant sur la mesure de son volume. D’autres pistes de recherche
avec l’IRM sont aussi développées, comme la cartographie de
l’accumulation de sodium dans certaines régions du cerveau, un phénomène
propre à l’Alzheimer. | |
|