Capsule outil: L’imagerie cérébrale
Pour comprendre la structure et le rôle des différentes parties
du cerveau, on a dû s’en remettre pendant longtemps à des méthodes
indirectes. La dissection post-mortem de sujets sains ou ayant souffert de certains
déficits suite à une lésion cérébrale localisée
nous a permis de faire certaines déductions quant aux implications fonctionnelles
de telle ou telle structure.
La destruction sélective de certaines
régions cérébrales chez l’animal a aussi permis de
confirmer le rôle de certaines structures bien conservées au cours
de l’évolution. Plus récemment, vers le milieu du siècle
passé, des stimulations électriques appliquées directement
sur le cerveau lors de neuro-chirurgies a permis à des chercheurs comme
Wilder Penfield d’établir les premières cartes cérébrales
fonctionnelles chez l’humain.
Depuis le début des années 1990, différentes techniques
d’imagerie cérébrale ont révolutionné cette
quête en permettant de « voir le cerveau penser » en temps réel.
Si ces techniques nous montrent ce qui se passe dans le cerveau au cours d’une
tâche sans avoir à ouvrir la boîte crânienne, c’est
surtout grâce aux progrès de l’informatique et de la détection
des rayonnements qui ont eu lieu à la fin du Xxe siècle.
On distingue généralement l’imagerie anatomique de l’imagerie
fonctionnelle. La première est conçue pour mettre en valeur les
structures cérébrales et tout ce qui peut venir les perturber (tumeurs,
hémorragies, caillots ou autres déformations présentes à
la naissance).
L’imagerie fonctionnelle mesure pour sa part l’activité
de certaines régions du cerveau durant certaines tâches. On l’utilise
surtout pour la recherche fondamentale qui vise à mieux comprendre le rôle
de nos diverses structures cérébrales, mais aussi pour diagnostiquer
des foyers épileptiques ou avant des opérations chirurgicales pour
identifier les aires cérébrales au rôle essentiel à
garder intactes à tout prix.
Une technique d’imagerie anatomique
est cependant très souvent utilisée de pair avec une technique fonctionnelle
pour mieux cerner l’anatomie et la fonction d’une aire cérébrale
chez un individu particulier.
Voici donc un bref aperçu
des techniques d’imagerie actuellement les plus employées :
| Imagerie structurelle | Imagerie fonctionnelle |
CT scan Imagerie par résonance magnétique (IRM) | |
| Technique de stimulation | |
Stimulation magnétique transcrânienne (SMT) | Le magnétoencéphalographe (MEG) |
Liens généraux sur l’imagerie cérébrale :
CT scan
Le CT scan vient de l’anglais « computerized tomography »
indiquant bien l’essence du CT scan : une série de radiographie mises
en valeur par ordinateur. Disponible depuis 25 ans, le CT scan a subi beaucoup
d’améliorations techniques qui en fait aujourd’hui l’une
des méthodes d’imagerie les plus employées.
Le CT
scan produit un réarrangement par ordinateur de plusieurs images prises
aux rayons X selon différents angles. Il obtient ainsi une bien meilleure
résolution que les rayons X classiques et peut donc déceler des
tumeurs ou des lésions à un stade plus précoce.
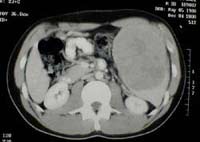
CT scan montrant une rate hypertrophiée par une
tumeur cancéreuse (à droite).
Source : Dr. Bob Richmond
La reconstitution par ordinateur permet aussi d’enlever les «
ombres » que d’autres parties du corps peuvent jeter sur la région
d’intérêt. Ceci est rendu possible par la source des rayons
X qui tourne autour du patient, photographiant ainsi l’organe cible sous
différents angles. Chaque tour produit ainsi une « tranche »
photographique, autrement dit l’image d’une coupe transversale de
l’organe. Après plusieurs tours, l’ordinateur devient en mesure
d’additionner les tranches pour créer une image tridimensionnelle
de l’organe.
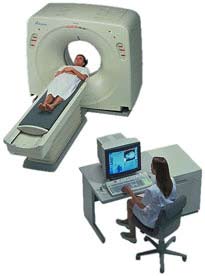
L’appareil
a la forme d’un beigne et l’organe à investiguer est placé
au centre du trou de ce « beigne ». Comme pour les rayons X, le patient
est exposé à une faible quantité de radiation durant le scan.
Le système d’émission de rayon X tourne autour du patient
et le détecteur est placé exactement à l’opposé
de la source. Il détecte ainsi les rayons X qui ont été absorbés
différemment après leur passage à travers les différents
tissus.
Dépendamment de ses symptômes, on peut injecter
ou faire boire au patient un colorant pour augmenter le contraste entre les tissus
normaux et anormaux. Les CT scan sont habituellement passés pour suivre
la récupération d’une chirurgie, d’une radiothérapie
ou d’une chimiothérapie pour des tumeurs cérébrales,
pour détecter les caillots, etc.
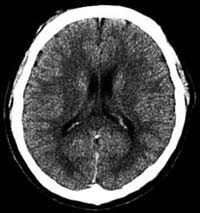
CT scan d’un cerveau normal.
Grâce à l’ordinateur, le CT scan peut donc créer
une vue tridimensionnelle à la fois des os et des tissus mous à
l’intérieur de laquelle on peut avancer ou reculer à loisir
pour en faire l’examen détaillé.
Les dernières
générations de CT scan génèrent leurs images suite
à un mouvement hélicoïdal de la source de radiation autour
du sujet au lieu d’une série de trajectoires circulaires, ce qui
permet d’aller plus vite et d’obtenir une définition encore
meilleure.
| Retour au sommaire des techniques d'imagerie |
L'imagerie
par résonnance magnétique (IRM)
L’avènement
de l’IRM à la fin des années 1970 a eu l’effet d’une
bombe dans le milieu médical. Cette nouvelle technique n’utilisait
ni les rayon X, ni les ultrasons, mais faisait plutôt appel aux champs magnétiques
en exploitant des propriétés physiques de la matière au niveau
sub-atomique, en particulier de l’eau qui constitue environ les trois quart
de la masse du corps humain.
L’IRM, en plus d’une définition
supérieure au CT scan, permet aussi d’obtenir non seulement des coupes
axiales du cerveau comme le CT scan, mais aussi des coupes sagittales et coronales.
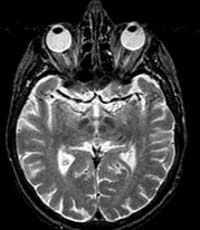
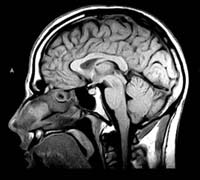
Le
fonctionnement de l’IRM est assez complexe, mais on peut en résumer
les grandes étapes ainsi :
- le champ magnétique de l’appareil de résonance magnétique va aligner celui, beaucoup plus faible, de chaque proton des atomes d’hydrogène contenus dans l’eau des différents tissus de l’organisme;
- la région dont on veut avoir une image est ensuite bombardée par des ondes radios;
- à l’arrêt des ondes radios, les protons retournent à leur alignement original en émettant un faible signal radio (la fameuse «résonance magnétique»);
- l’intensité de la résonance magnétique est proportionnelle à la densité des protons dans le tissu, et par conséquent à son taux d’hydratation ;
- des capteurs spéciaux relaient cette information à un ordinateur qui combine ces données pour créer des images de coupe du tissu dans différentes orientations.
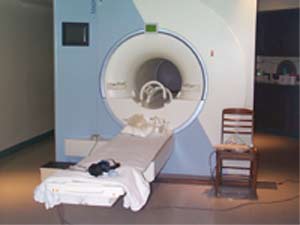
Le
sujet couché sur une table coulissante est introduit dans un tunnel à
peine plus large que ses épaules. Ce tunnel contient les fils qui créent
le champ magnétique ainsi que les capteurs d’onde radio.
Comme l’immobilité du sujet est très importante pour la clarté
des images, la tête est attachée pour en limiter les mouvements.
Le bruit assez fort provoqué par l’IMR est contré à
l’aide de bouchons pour les oreilles.
Avant de pénétrer
dans le scan (et même dans la pièce où est le scan), le sujet
doit se départir de tout objet métallique puisque ceux-ci pourraient
être attirés par le champ magnétique. Les gens possédant
des prothèses, des clips artérielles ou des « pacemaker »
cardiaque doivent aussi éviter l’IMR pour des raisons évidentes.
Bien que l’utilisation du CT scan soit encore prédominante pour
la poitrine et l’abdomen, l’IRM est l’outil de prédilection
pour le cerveau, les extrémités des membres et la colonne vertébrale.
Les tissus malades ou endommagés contiennent généralement
plus d’eau ce qui permet de les détecter avec l’IRM.
Comme pour le CT scan, une substance contrastante peut être injectée
: il s’agit la plupart du temps de composés du gadolinium qui joue
pour l’IRM le même rôle que l’iode, mais avec moins de
risques d’incidents allergiques.
|
|
L'électroencéphalographie
L’électroencéphalographie (EEG) permet d’amplifier
l’activité électrique générées par les
neurones. En effet, plusieurs fonctions cognitives ou motrices produisent des
patterns activité neuronale caractéristiques qui provoquent une
signature particulière sur l’électroencéphalogramme.
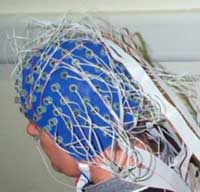
L’EEG mesure donc l’activité neuronale globale et continue
du cerveau grâce à des électrodes collées à
la surface du cuir chevelu. Les ordinateurs actuels permettent d’analyser
l’activité cérébrale captée par plusieurs douzaines
d’électrodes situées à différents endroits sur
le crâne.
Les
courants recueillis sont surtout ceux générés au niveau des
dendrites des neurones pyramidaux que l’on retrouve massivement dans le
cortex. Ceux-ci ont une orientation parallèle, ce qui amplifie le signal
de leur activité commune.
On peut donc considérer les oscillations
de l’EEG comme la somme de différentes oscillations produites par
différentes assemblées neuronales, chacune de ces « harmoniques
» se superposant pour produire le tracé global enregistré.
Celui-ci offre d’ailleurs pour l’analyse les deux mêmes caractéristiques
que les ondes sonores : la fréquence d’oscillation et son amplitude.
Les fréquences des ondes cérébrales s’étendent
de 0.25 Hz à environ 60 Hz (1 Hertz étant une oscillation par seconde).
L’état de conscience de la personne (éveil, sommeil, rêve…)
a une importance déterminante sur la fréquence de l’électroencéphalogramme.
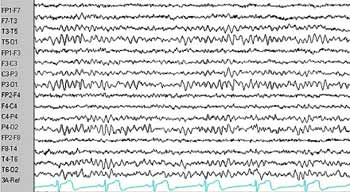
EEG normal
Des profils de fréquences
s’apparentant à certaines activités ont pu être établis.
Ainsi, on distingue les ondes :
DELTA: <4 hz (sommeil profond, coma)
;
THETA: 4-8 hz (activité limbique: mémoire et émotions)
;
ALPHA: 8-12 hz (sujet alerte, sans toutefois un traitement actif de l’information,
prédominant surtout dans les lobes occipitaux et frontaux, par exemple
lorsque les yeux sont clos) ;
BETA: 13-30hz (sujet alerte et traitant activement
de l’information) ;
GAMMA: >30-35 hz (pourrait être relié
à la conscience, c’est-à-dire le lien entre différentes
régions cérébrales pour former un concept cohérent).
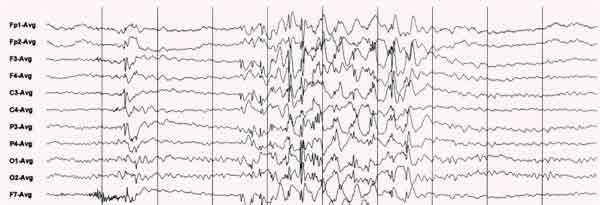
EEG d'une crise d'épilepsie généralisée.
L’EEG offre une excellente résolution temporelle et un coût
relativement moins élevé que l’IRMf ou le PET scan, mais sa
résolution spatiale demeure toutefois pauvre. Malgré tout, l’EEG
peut aider à diagnostiquer des foyers épileptiques, des tumeurs
cérébrales, des lésions, des caillots, etc. Il aide aussi
à trouver l’origine de migraines, de problèmes d’étourdissements,
de somnolence, etc.
Les cartographies cérébrales faites
avec l’EEG utilisent aussi fréquemment ce que l’on appelle
des « potentiels évoqués ». Il s’agit d’une
procédure où l’on soumet le sujet à un stimulus particulier
(une image, un mot, une stimulation tactile…) de façon à enregistrer
une réponse neuronale associée à ce stimulus dans le cerveau.
Une autre technique proche de l’EEG est la magnétoencéphalographie
(MEG). Comme l’EEG, la MEG enregistre les oscillations neuronales du cerveau,
mais elle le fait par l’entremise des faibles champs magnétiques
émis par cette activité plutôt que par leur champ électrique.
| Retour au sommaire des techniques d'imagerie |
Imagerie par résonance magnétique fonctionnelle (IRMf)
À la différence de la résonance magnétique qui permet de visualiser l’anatomie des structures cérébrales, l’imagerie par résonance magnétique fonctionnelle (IRMf) nous renseigne sur l’activité des différentes régions cérébrales. L’appareillage qui entoure le sujet et le fonctionnement de base est sensiblement le même qu’avec l’IRM, mais les ordinateurs qui analysent le signal diffèrent.
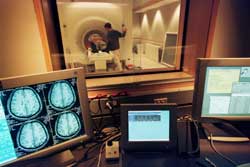
Photo by: Jeff Miller
Source: The science of Emotions,
research at the University of Wisconsin-Madison
Le phénomène
physiologique sur lequel s’appuie l’IRMf (tout comme la TEP
d’ailleurs) fut mis en évidence à la fin du 19ème siècle
lorsque des neurochirurgiens établirent que les fonctions cognitives modifient
localement la circulation sanguine cérébrale. En effet, quand un
groupe de neurones devient plus actif, une vasodilatation locale des capillaires
sanguins cérébraux se produit automatiquement pour amener davantage
de sang, et donc d’oxygène, vers ces régions plus actives.
Or l’hémoglobine, cette protéine possédant
un atome de fer qui transporte l’oxygène, a des propriétés
magnétiques différentes selon qu’elle transporte de l’oxygène
ou qu’elle en a été débarrassée par la consommation
des neurones les plus actifs. C’est la concentration de désoxy-hémoglobine
(l’hémoglobine débarrassée de son oxygène) que
l’IMRf va détecter. En effet, cette molécule a la propriété
d’être paramagnétique : sa présence engendre dans son
voisinage une faible perturbation du champ magnétique.
Sans entrer
dans les détails, mentionnons que l’augmentation du débit
sanguin cérébral dans une région plus active du cerveau est
toujours supérieure à la demande d’oxygène accrue de
cette région. Par conséquent, c’est la baisse du taux de désoxy-hémoglobine
(diluée dans un plus grand volume de sang oxygéné) que l’IRMf
va faire correspondre à une augmentation de l’activité de
cette région.
En soustrayant par la suite l’intensité
des différentes régions de cette image d’une autre qui a été
préalablement enregistrée avant la tâche à accomplir,
on observe une différence dans certaines zones qui « s’allument
» aux régions les plus irriguées et donc les plus actives
au niveau de l’activité neuronale.
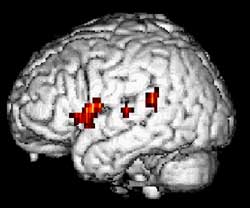
Résonance magnétique fonctionnelle d’une
femme de 24 ans durant une tâche de génération de mots.
(Source : Dept. Neurology and Radiology, Münster)
L’IRMf a été développé au début des années
1990 lorsque des ordinateurs de plus en plus puissants furent couplés aux
appareils d’IRM. Le temps d’enregistrement peut être aussi court
que 40 millisecondes et la résolution de l’ordre du millimètre
est la meilleure de toutes les techniques d’imagerie fonctionnelle. Les
derniers scanners d’IRMf peuvent produire quatre photos par seconde du cerveau,
ce qui permet de suivre le déplacement de l’activité neuronale
au cours d’une tâche complexe.
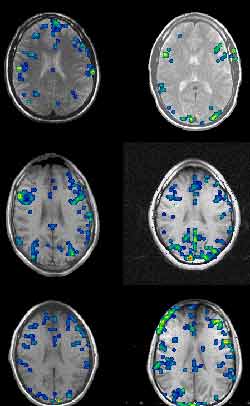
Résonance magnétique fonctionnelle durant
le test de Stroop pour six sujets différents démontrant la grande
variabilité entre les participants. (Source : Dr. David C. Osmon)
L’IRMf,
qui peut être utilisée sans l’injection de colorant dans l’organisme
du sujet, est très appréciée en recherche fondamentale. Un
autre de ses grands avantages est que la même machine peut fournir une image
structurelle et fonctionnelle du même cerveau, facilitant ainsi les correspondances
anatomo-fonctionnelles.
L’IRMf est souvent considéré
comme la technique d’imagerie produisant les résultats les plus impressionnants.
Mais les coûts de ces appareils et leur entretien sont aussi impressionnants,
de sorte que son utilisation doit souvent être partagé et il y a
souvent des listes d’attentes.
|
L’imagerie cérébrale sous le feu des critiques La « réutilisation neuronale » pour enfin sortir de la phrénologie ? Une
marche en milieu naturel plutôt qu’urbain diminue vos
idées noires |
La tomographie par émission de positons (TEP)
La tomographie par émission de positons (TEP), mieux connue sous son appellation anglaise de « PET scan », fut la première technique d’imagerie cérébrale fonctionnelle à voir le jour au milieu des années 1970.

Le
phénomène physiologique sur lequel s’appuie la TEP (tout comme
l’IRMf d’ailleurs)
fut mis en évidence à la fin du 19ème siècle lorsque
des neurochirurgiens établirent que les fonctions cognitives modifient
localement la circulation sanguine cérébrale. En effet, quand un
groupe de neurones devient plus actif, une vasodilatation locale des capillaires
sanguins cérébraux se produit automatiquement pour amener davantage
de sang, et donc d’oxygène, vers ces régions plus actives.
Lors d’une TEP, on doit injecter au sujet une solution contenant un
élément radioactif qui peut être l’eau elle-même
ou du glucose radioactif par exemple. Davantage de radioactivité sera donc
émise des zones cérébrales les plus active à cause
de cette vasodilatation qui amène plus de solution radioactive dans ces
régions.
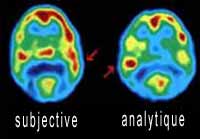
Une écoute subjective ou analytique d’une
même pièce de musique par le même sujet active préférentiellement
l’hémisphère droit ou l’hémisphère gauche.
Les fameux positons de la TEP proviennent de la dégradation de ce
noyau radioactif incorporé dans le système sanguin du sujet. Un
positon est une particule élémentaire ayant la même masse
qu’un électron mais une charge de signe opposé.
Les
positons émis par la dégradation radioactive vont immédiatement
s’annihiler avec les électrons des atomes voisins. Cette annihilation
produit de l’énergie qui prend la forme de deux rayons gamma émis
dans des directions diamétralement opposées.
Une série
de détecteurs placés autour de la tête du sujet va ensuite
enregistrer les couples de rayons gamme émis et, grâce aux calculs
faits par l’ordinateur, identifier la position de leur lieu d’émission.
L’ordinateur pourra ainsi, après de nombreux calculs, reconstituer
l’image globale du cerveau et de ses zones les plus actives.
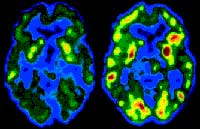
PET scan du cerveau d’un alcoolique 10 jours (à
gauche) et 30 jours (à droite) après le début de l’abstinence.
Comme la demie-vie des éléments radioactifs employés
doit être courte (environ deux minutes), ceux-ci doivent être produits
sur place, ce qui implique des coûts assez élevés et limite
l’accessibilité des scans à TEP.
En plus de montrer
l’activation fonctionnelle du cerveau ou de détecter des tumeurs
ou des caillots, la particularité de la TEP est de permettre d’inclure
l’isotope radioactif dans certaines substances dont on veut connaître
l’utilisation métabolique par certaines régions cérébrales.
L’étude des neurotransmetteurs a bénéficié d’une
façon importante de cette approche qui a permis de préciser la distribution
de plusieurs d’entre eux.
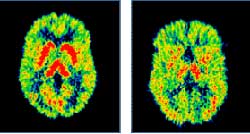
L’image de gauche montre la TEP du cerveau d’un
sujet normal. À droite, la TEP révèle un taux de sérotonine
(un neurotransmetteur) plus faible chez un sujet atteint de dépression
sévère.
Les images produite par la TEP
ne rivalisent pas avec celles de l’IRMf en terme de résolution, mais
offrent souvent des contrastes de couleurs spectaculaire (les couleurs les plus
chaudes correspondant aux zones les plus actives).
Le temps efficace
pour tester une tâche est relativement court (moins d’une minute)
à cause de la dégradation rapide de la source de radioactivité.
Après chaque tâche, le sujet doit attendre plusieurs minute pour
que le niveau de radioactivité émis soit négligeable avant
de recevoir une nouvelle dose pour la tâche suivante.
Les doses
de radioactivité reçues par un sujet durant une session de TEP sont
peu élevées, mais on ne permet tout de même qu’une seule
session par année à un même sujet.
|
|
Stimulation magnétique transcrânienne (SMT)
La SMT fut introduite
au milieu des années 1980 pour étudier les voies motrices qui partent
du cortex moteur et descendent dans la moelle épinière jusqu’aux
muscles. Mais on savait stimuler des nerfs avec des champs magnétiques
depuis le début des années 1960.
Les nouvelles techniques
de SMT permettent cependant d’appliquer un courant électrique directement
dans le cerveau. Mais aucune opération chirurgicale n’est requise
comme pour la stimulation avec une électrode puisqu’on utilise un
champ magnétique qui passe directement à travers le crâne
sans aucune douleur.
Le champ magnétique est généré
par un courant qui circule à travers une bobine de fils de cuivre isolée
dans une gaine de plastique. La bobine, qui ressemble à une grosse cuillère,
est placée juste au-dessus du crâne, au-dessus de la région
cérébrale à stimuler.
Le champ magnétique
généré par le courant traverse facilement le crâne
et produit à son tour un courant électrique local dans le cerveau
du sujet. La profondeur de la stimulation est cependant limitée à
environ deux centimètres sous la surface du crâne à cause
de l’atténuation rapide du champ magnétique avec la distance.
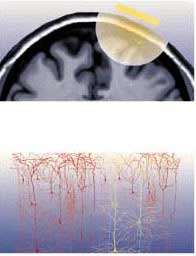
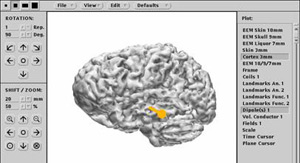
La positionnement précis de la bobine de SMT au-dessus de la région cérébrale d’intérêt est très important. Pour ce faire, on a souvent recours à une résonance magnétique du cerveau du sujet pour s’adapter à ses circonvolutions cérébrales particulières. Des appareils stéréotaxiques utilisent ensuite certains repères visibles à la fois sur le sujet et sur son IRM (comme le pont du nez par exemple) pour positionner la bobine de SMT exactement au bon endroit.
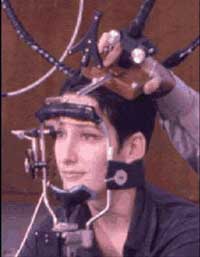
Bobine de SMT montée sur un appareil stéréotaxique
qui permet de la positionner au-dessus de la zone d’intérêt,
ici cortex frontal supérieur gauche du sujet. Le même système
peut être installé sur la tête d’un sujet dans un PET
scan.
Source: ICBM et le Dr. Roger Woods, UCLA.
La
SMT est souvent utilisée conjointement avec d’autre techniques d’imagerie
cérébrale dans les études de cartographie fonctionnelle du
cerveau. On s’en sert par exemple pour produire une réponse physiologique
sans équivoque (une contraction musculaire par exemple) ou, au contraire,
pour créer une « lésion virtuelle » temporaire. Cette
dernière est produite lors d’une tâche en interférant
avec la région cérébrale identifiée comme étant
active durant cette tâche.
La SMT à répétition
est une variante plus récente de la SMT où le champ magnétique
peut être répété à des fréquences relativement
élevées. Utilisée plusieurs minutes par jour pendant plusieurs
semaines, cette technique pourrait avoir des effets antidépresseurs lorsqu’elle
est appliquée à des régions cérébrales spécifiques
selon des paramètres de stimulation adéquats.
Des portes d’entrée pour découvrir votre cerveau De l’importance des oscillations cérébrales lentes durant le sommeil profond Stimuler
ou inactiver des régions cérébrales, d’hier
à aujourd’hui |