|
|
| Le financement de ce site est assuré par vos dons, merci! | |
|
|
|
|
|||||
|
|
|||||||
|
|
|
|
| |
Malbouffe
et Alzheimer : des liens plus étroits qu’on pensait De l’importance des oscillations cérébrales lentes durant le sommeil profond Ce qui est bon pour le cerveau en 6 points dont 3 encore confirmés Expliquer la science non pas à trois niveaux de difficulté mais à cinq ! Le système glymphatique : les égouts du cerveau Le « corps-cerveau » sous toutes ses coutures
Deux systèmes de pensée dans le même cerveau ?
| |
Il est toujours difficile de distinguer les premiers stades d’une démence du vieillissement normal. La difficulté tient au fait que les premiers symptômes des démences apparaissent très graduellement, souvent à l’insu de la personne atteinte. Dans le cas de la plus fréquente des démences, celle de type Alzheimer, la dégénérescence neuronale à l’origine des déficits se déploie de façon séquentielle caractéristique dans le cerveau. De sorte que les symptômes de l’Alzheimer apparaissent dans un ordre qui, sans être complètement prévisible, est typique de cette démence. On utilise généralement les termes « léger, modéré et avancé » pour définir trois grands stades de l’évolution de la démence de type Alzheimer. Évidemment, les transitions entre ces différents stades ne sont pas coupées au couteau, pas plus que chaque patient va expérimenter les symptômes dans le même ordre, avec la même gravité ou la même durée (voir l’encadré ci-bas sur l'espérance de vie). Il n’empêche que les associations de personnes atteintes de ce type de démence ont identifié des signes précurseurs et des symptômes typiques qui apparaissent à peu près dans l’ordre suivant. La région de l’hippocampe dans les profondeurs du cortex temporal étant généralement la première touchée, il n’est pas étonnant de constater que les premiers symptômes consistent en des troubles de la mémoire. Ces derniers se manifestent initialement par des distractions mineures que l’on peut facilement confondre avec l’un des effets courant du vieillissement normal (oublier ses clés, un rendez-vous, le nom de quelqu’un, etc).
À ce stade léger (ou initial), les souvenirs plus anciens sont relativement préservés. Mais les oublis de choses récemment apprises deviennent fréquents et seront bientôt remarqués par les proches. Ceux-ci seront de plus en plus souvent questionnés, et parfois à plusieurs reprises, sur une date ou un événement à venir. On assiste aussi à l’utilisation plus fréquente de notes et d’aide-mémoire. Malgré cela, la victime de ces pertes de mémoire épisodique peut avoir tendance à les minimiser au début. Parmi les autres symptômes cognitifs qui peuvent apparaître durant ce premier stade, on retrouve une durée d’attention plus courte, de la difficulté à se concentrer, des erreurs de jugement et des problèmes d’orientation spatiale ou temporelle. Les patients ont par exemple tendance à errer ou à se perdre dans des endroits qui leur sont pourtant familiers. L’humeur et le comportement commencent aussi à être affectés, menant parfois à une exagération des traits de caractère de la personne (agressivité chez les colériques, passivité chez les placides, etc), à des sautes d’humeur, des états dépressifs ou à de la nervosité. La prise de conscience par moment de la détérioration de ses facultés peut devenir une source d’anxiété. De légers problèmes de coordination motrice peuvent survenir, mais en général, à ce stade initial, la personne atteinte continue à mener une vie relativement indépendante avec un minimum d’aide. On entre dans le stade modéré de la démence de type Alzheimer quand le jugement commence à être altéré au point où l’organisation des activités quotidiennes devient difficile. C’est le stade de la perte d’autonomie. La personne peut avoir par exemple de la difficulté à accomplir des tâches familières qu'elle a exécutées toute sa vie, comme préparer ses repas, faire sa toilette ou son budget. Les facultés cognitives comme la mémoire continuent de se détériorer et la personne a de plus en plus de mal à apprendre et à retenir de nouvelles informations. Leurs souvenirs de jeunesse et d’âge moyen sont toutefois encore préservés. Les plaques amyloïdes et la dégénérescence neurofibrillaire s’étendent progressivement aux régions impliquées dans le langage ainsi que dans la perception du corps parmi les objets qui l’entourent. D’où les difficultés dans les tâches quotidiennes, mais aussi dans la vie professionnelle et sociale qui souffrent énormément de la dégradation des facultés langagières : la moindre conversation devient laborieuse, la personne perd le fil de ses idées, ne trouve plus les mots pour s’exprimer, ne comprend pas bien ce qu’on lui explique. Elle délaisse alors au même moment la lecture et l’écriture. Avec l’évolution de la forme modérée vers la forme avancée, il n’est pas rare de voir apparaître des problèmes plus sévères et handicapants, comme de l’insomnie, des fluctuations de l’appétit ou des changements de la personnalité qui s’ajoutent au vécu déjà difficile du patient. Quand la démence de type Alzheimer atteint le stade avancé, la majeure partie du cortex est sérieusement endommagée. Les individus ont des difficultés graves à s’exprimer, à reconnaître leurs amis et même leurs proches. La confusion mentale, aggravée par une perte de mémoire sévère, donne souvent lieu à des hallucinations ou des délires paranoïdes. D'un point de vue comportemental, les patients deviennent souvent irritables ou indifférents, ont des gestes stéréotypés, pleurent ou rient sans raison apparente, ont des gestes déplacés, etc. Il ne faut pas oublier que deux personnes évaluées au même stade peuvent présenter des atteintes différentes, les facultés cognitives pouvant être plus touchées que l’autonomie comportementale, ou l’inverse. Au stade avancé, certains négligent souvent leur hygiène corporelle, peuvent oublier de manger, perdent le contrôle de leur vessie et de leurs intestins. À ce stade, une surveillance permanente par les proches ou l’hébergement dans un centre de soins devient nécessaire. Soutenir la personne atteinte pour lui assurer la plus grande qualité de vie possible devient alors l’objectif le plus important. Avec le temps, la démence de type Alzheimer devient souvent une « démence mixte », c’est-à-dire qu’elle cohabite avec d’autres formes de démence, comme la démence vasculaire et la maladie à corps de Lewy. Le patient peut mourir d’une autre maladie à n’importe quel stade de l’évolution de sa démence. Cependant, dans le stade avancé de la démence de type Alzheimer, beaucoup de décès sont causés par une infection secondaire. Un cas fréquent étant la pneumonie engendrée par de la salive ou de la nourriture que le patient, qui a de la difficulté à avaler, laisse entrer dans ses voies respiratoires.
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Malbouffe et Alzheimer : des liens plus étroits qu’on pensait
|
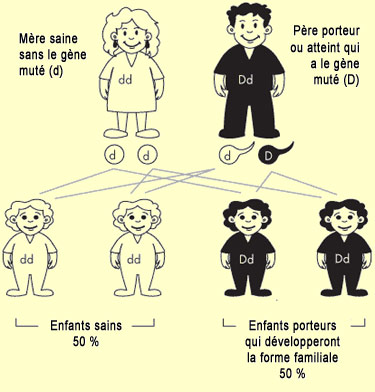
Bien que la recherche ait fait beaucoup progresser nos connaissances des mécanismes à l’œuvre dans la démence de type Alzheimer, ses causes ultimes demeurent méconnues. La recherche a toutefois permis de mettre en évidence des facteurs de risques (voir l’encadré). Comme pour d’autres maladies chroniques, ces facteurs de risque peuvent se combiner pour déclencher l’Alzheimer. Mais avant de considérer ces facteurs de risque environnementaux et génétiques, il faut noter qu’il existe deux formes de l’Alzheimer, la forme dite « sporadique » et la forme dite « familiale ». Cette dernière a tendance à avoir un déclenchement hâtif avec des déficits qui apparaissent entre 30 et 65 ans, contrairement à la forme sporadique qui débute habituellement après 65 ans. Mais outre cette différence, les deux affections sont en tout point similaires au niveau de la nature des symptômes et des anormalités cérébrales et biochimiques observées. Ce qui les distingue surtout, c’est d’abord leur fréquence relative : la forme sporadique représente l’immense majorité des cas alors que la forme familiale est beaucoup plus rare avec 5 à 7 % des cas environ. Par ailleurs, la forme sporadique n’a pas de composante héréditaire décisive, tandis que la forme familiale est fortement déterminée par certains gènes. Quand on parle des facteurs de risque de l’Alzheimer, il faut donc d’abord préciser laquelle de ses formes on considère, puisque les facteurs de risque génétique sont très différents pour les deux formes. Pour la forme familiale d’abord, ce sont les gènes qui déterminent en grande partie l’avènement de la démence. On en a identifié trois, sur trois chromosomes différents : le gène de la protéine précurseur de l’amyloïde (APP) sur le chromosome 21, le gène préséniline 1 (PS1) sur le chromosome 14 et le gène préséniline 2 (PS2) sur le chromosome 1. Une personne va développer la forme familiale de l’Alzheimer si elle hérite d’un seul de ces gènes rendus défectueux par une mutation. Ces gènes mutés produiront à leur tour des protéines défectueuses, et plusieurs indices portent à croire que ces dysfonctionnements conduisent à une augmentation d’une forme de protéines bêta-amyloïde qui s’accumule en plaques toxiques dans le cerveau. Il s’agit donc d’une dysfonction « autosomale dominante ». « Autosomale », parce que les gènes impliqués ne sont pas situés sur un chromosome sexuel X ou Y (déterminant le sexe d’une personne), et « dominante » parce que la personne n’a besoin que d’une copie du gène muté pour en souffrir. Une personne qui hérite d’un de ces gènes mutés développe donc systématiquement l’Alzheimer et la transmet à la moitié de sa descendance. Autrement dit, un enfant ayant un parent atteint de la forme familiale de l’Alzheimer aura une probabilité de 50 % d’en hériter lui aussi.
Cela étant dit, il n’y a qu’environ la moitié des cas d’Alzheimer à « déclenchement hâtif » qui sont dus aux mutations de la forme familiale. Et même si plusieurs membres d’une même famille sont touchés par l’Alzheimer, cela ne signifie pas forcément qu’il s’agisse de la forme familiale. Cela pourrait être la forme sporadique, qui n’est pas complètement indépendante des antécédents familiaux. Car on sait aujourd’hui que même dans le cas de la forme sporadique, le fait d'avoir un parent proche (père, mère, frère ou soeur) atteint de l'Alzheimer augmente le risque de développer celle-ci. Il existe donc des facteurs génétiques à risque pour la forme sporadique, c’est-à-dire des gènes qui ne causent pas directement l’Alzheimer comme pour la forme familiale, mais qui sont plus fréquents chez les personnes atteintes, bien qu'on les retrouve aussi chez des sujets normaux. Si plusieurs gènes sont suspectés d’être des facteurs de risque pour la forme sporadique de l’Alzheimer (CLU, CR1, etc), le plus connu est sans conteste l'allèle 4 du gène de l'apolipoprotéine E (APOE4) découvert en 1993 sur le chromosome 19. Ce gène APOE contribue à la fabrication d’une protéine qui aide à transporter le cholestérol dans le corps, et différentes explications ont été proposées pour expliquer ses effets néfastes dans l’Alzheimer. Le gène APOE a trois allèles principaux, e2, e3 et e4. Il s’agit de trois versions du gène qui, sans être des mutations délétères conduisant à des protéines dysfonctionnelles comme pour la forme familiale de l’Alzheimer, sont des variantes plus ou moins efficaces qui sont apparues au fil de l’évolution. Dans le cas du gène de l’APOE, on retrouve ses variantes dans la population dans des proportions connues : 51% pour l’APOE2, 80 % pour l’APOE3 et 15 % pour l’APOE4. La forme la plus commune, e3, n’a pas d’effet sur l’incidence de l’Alzheimer. L’allèle e2 pourrait, quant à lui, diminuer l’incidence de l’Alzheimer chez ceux qui le possèdent. Ce sont les personnes qui ont l’allèle e4 sont plus susceptibles de développer l’Alzheimer. Comme tous nos gènes sont en deux copies (l’une en provenance de la mère, et l’autre du père), ceux qui n’héritent que d’une copie de APOE4 voient leur risque d’Alzheimer augmenter de trois fois environ. Pour ceux dont les deux copies sont e4, le risque est multiplié environ par onze. Cela revient à dire qu’à 65 ans, environ la moitié de ces derniers auront une démence de type Alzheimer. La présence de l' APOE4 n'est donc ni nécessaire ni suffisante pour développer la maladie d'Alzheimer, mais le risque augmente avec le nombre d’allèles e4. Cela veut non seulement dire qu’une personne qui est porteuse de deux gènes de l’APOE4 n'en sera pas nécessairement atteinte, mais aussi qu’une personne qui n'est porteuse d’aucun allèle e4 peut quand même développer l'Alzheimer. L’autre grand facteur de risque de la forme sporadique de l’Alzheimer pour ces personnes sans APOE4, comme d’ailleurs pour ceux qui en ont, est tout simplement l’âge. L’âge est en effet considéré comme le facteur de risque le plus important pour le développement de l’Alzheimer. Car même si ce type de démence peut apparaître avant 50 ans, la plupart des personnes atteintes ont plus de 65 ans. Chose certaine, aucun adolescent n’est atteint. Il semble qu’en vieillissant, les mécanismes naturels de réparation du cerveau perdent de leur efficacité, un déclin dont l’importance peut toutefois varier selon les individus. De plus, d’autres facteurs de risque reconnus pour augmenter avec l'âge comme l’hypercholestérolémie ou le surpoids, sont aussi des facteurs de risque reconnus. Le sexe est également un facteur de risque de l’Alzheimer. En l’occurrence, le sexe féminin, puisque deux fois plus de femmes que d'hommes sont atteintes d'Alzheimer au-delà de 65 ans. Comme les femmes vivent en moyenne plus longtemps que les hommes et que l'âge est un facteur de risque de l’Alzheimer, cette longévité accrue des femmes explique sans doute au moins partiellement l’écart observé. D’autant plus que les femmes âgées se retrouvent ainsi davantage exposées à des maladies dont la prévalence augmente avec l’âge comme le diabète, qui est aussi un facteur de risque de l’Alzheimer. La diminution du taux d’œstrogène qui survient à la ménopause est aussi évoquée pour expliquer le risque accru de l’Alzheimer chez la femme, cette hormone ayant des effets protecteurs sur le cerveau. Enfin, au début de 2009, une étude a mis en évidence un premier gène qui favoriserait l’Alzheimer chez la femme. Il s’agit d’une variante du gène de la protéine PCDH11X, qui se trouve sur le chromosome sexuel X, celui dont les femmes possèdent deux copies et les hommes seulement une (le chromosome qui complète la paire chez l’homme étant le Y, reçu de leur père). L’étude montre que ce ne sont que les femmes qui ont ce gène PCDH11X anormal sur leurs deux chromosomes X qui ont un risque plus élevé de développer l’Alzheimer. De nombreux autres facteurs de risque ont été répertoriés pour l’Alzheimer. Des liens étroits existent par exemple entre les facteurs de risque des maladies cardiovasculaires et ceux de l’Alzheimer. L’hypertension ou un taux de cholestérol trop élevé sont en effet des facteurs susceptibles de déclencher ou d’accélérer l’Alzheimer. Et de fait, il semble qu’un contrôle efficace des problèmes d’hypertension ou d’hypercholestérolémie réduit le risque d’apparition de l’Alzheimer chez les patients traités et en ralentit la progression chez les personnes déjà atteintes. La découverte qu’une version défectueuse du gène SORL1 semble impliquée dans certains cas d’Alzheimer renforce d’autant plus ce lien puisque ce gène est également relié au cholestérol. Cette variante du gène SORL1 fabrique en moins grande quantité le récepteur de la protéine APOE, elle aussi clairement associée au métabolisme du cholestérol et aux plaques amyloïdes de l’Alzheimer. On a aussi déjà mentionné le diabète (celui « de type 2 » (adulte)) comme autre facteur de risque de l'Alzheimer, notamment à cause des problèmes cardiovasculaires qui lui sont associés. On sait par ailleurs que le glucose est moins bien assimilé dans le cerveau d'une personne souffrant d'Alzheimer, exactement comme un diabétique va mal assimiler le glucose dans son organisme. Sans être diabétique au sens habituel du terme, il semble que la personne souffrant d’Alzheimer ait une production réduite d'insuline dans le cerveau et que ses neurones y sont moins sensibles (la production de l'insuline dans le cerveau étant indépendante de celle dans l’organisme). Le stress est un facteur de risque de l’Alzheimer par l’entremise du cortisol dont l’effet délétère sur les populations neuronales est bien connu. Comme le stress accélère aussi le vieillissement tissulaire par l’entremise d’une plus grande production de radicaux libres, il favorise aussi l’Alzheimer dont l’âge est un facteur de risque si important. Les liens intimes entre stress chronique, inhibition de l’action et dépression font aussi en sorte que celle-ci se voit souvent associée aux facteurs de risque de l’Alzheimer. Les accidents cérébraux vasculaires (ACV), y compris les « mini-ACV » peuvent favoriser l’avènement plus précoce de démences vasculaires mais également de type Alzheimer. Même chose pour les traumatismes graves à la tête, souvent accompagnés de pertes de conscience (les commotions à répétition chez les boxeurs, par exemple). Des études ont démontré que les personnes ayant moins de six ans de scolarité semblent être plus susceptibles à l’Alzheimer. Mais il se pourrait aussi que des facteurs associés à cette faible scolarité, tels de bas revenus entraînant un mode de vie malsain, puissent expliquer cette susceptibilité. De manière plus
générale, le peu de stimulation intellectuelle
ou d’activité physique a ici, comme pour bien d’autres
pathologies, un effet aggravant. |
| |
|
|
|
|
|
|
|
|